Los investigadores del Laboratorio Nacional Lawrence Berkeley (Berkeley Lab) del Departamento de Energía de los Estados Unidos están ahora en el proceso de un gran avance hacia la fotosíntesis artificial. Son bastante optimistas sobre las propiedades de los cristales nanométricos de óxido de cobalto. Están apostando por el óxido de cobalto que puede llevar a cabo eficazmente la crucial reacción fotosintética de dividir las moléculas de agua.
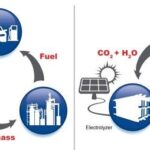
La fotosíntesis artificial no se sumará a los gases de efecto invernadero y, por lo tanto, al calentamiento global. Este será un recurso renovable para la energía del transporte. La idea es crear una hoja artificial que pueda duplicar los pocos pasos de la fotosíntesis. Esa hoja puede capturar los fotones solares y tener un sistema catalítico que puede oxidar el agua.
Heinz Frei y Feng Jiao han publicado los resultados de su estudio en la revista Angewandte Chemie. Esta investigación se llevó a cabo con la ayuda del Helios Solar Energy Research Center (Helios SERC), un programa científico del Berkeley Lab bajo la dirección de Paul Alivisatos. Se están concentrando en el desarrollo de combustibles a partir de la luz solar. Frei es el subdirector de Helios SERC.
Heinz Frei, químico de la División de Biociencias Físicas del Berkeley Lab, explica: «La fotooxidación de moléculas de agua en oxígeno, electrones y protones (iones de hidrógeno) es una de las dos medias reacciones esenciales de un sistema de fotosíntesis artificial: proporciona los electrones necesarios para reducir el dióxido de carbono a un combustible».
De nuevo enfatizó por qué está poniendo mucho esfuerzo en el óxido de cobalto, «La fotooxidación efectiva requiere un catalizador que sea eficiente en su uso de fotones solares y lo suficientemente rápido como para mantenerse al día con el flujo solar para evitar el desperdicio de esos fotones.
Los racimos de nanocristales de óxido de cobalto son suficientemente eficientes y rápidos, y también son robustos (duran mucho tiempo) y abundantes. Encajan perfectamente en la cuenta».
Fredi también explicó por qué no están muy interesados en el uso del óxido de iridio para la fotosíntesis artificial. Afirmó que aunque el óxido de iridio es eficiente y lo suficientemente rápido para la absorción de la luz y un buen catalizador, este metal es el menos abundante en la tierra. Por lo tanto, no es muy práctico utilizarlo a escala comercial.
Él dice: «Necesitábamos un metal que fuera igualmente efectivo pero mucho más abundante». Primero intentaron tomar los complejos organometálicos a base de manganeso para la fotosíntesis artificial, que las plantas utilizan en el Photosystem II. Pero los compuestos que contenían manganeso eran insolubles en agua y no muy robustos.
Fredi y su equipo prestaron atención al óxido de cobalto, que es un material muy abundante y apto para uso comercial. El óxido de cobalto también se disuelve en agua.
Pero no fue una historia de éxito desde el principio. Las partículas de óxido de cobalto de tamaño micrónico eran ineficaces y tardaban en actuar como catalizadores. Entonces Frei y Jiao se volvieron al óxido de cobalto de tamaño nanométrico.
«El rendimiento de los grupos de cristales de óxido de cobalto (Co3O4) de tamaño nanométrico fue unas 1.600 veces mayor que el de las partículas de tamaño micrométrico», dijo Frei. «Y la frecuencia de rotación (velocidad) fue de alrededor de 1.140 moléculas de oxígeno por segundo por cúmulo, lo que es proporcional al flujo solar a nivel del suelo (aproximadamente 1.000 vatios por metro cuadrado)».
El siguiente gran paso, sin embargo, será integrar la media reacción de oxidación del agua con el paso de reducción de dióxido de carbono en un sistema de tipo hoja artificial.